トシリズマブ _ アクテムラの副作用と効果:関節リウマチ治療の安全性
Di: Stella
トシリズマブは、以下の治療に承認されています。 ・重篤または生命を脅かすサイトカイン放出症候群(CRS)。キメラ抗原受容体(CAR)T細胞療法に起因するCRSを有する成人患者お トシリズマブは、IL-6のシグナル伝達を阻害することによって抗リウマチ効果を示す薬剤である。 2008年4月に本邦でRAの適応が承認された。 アクテムラによる治療(関節リウマチ(RA), 若年性特発性関節炎(JIA), 成人発症スチル病(AOSD), 高安動脈炎(TAK)・巨細胞性動脈炎(GCA), キャッスルマン病(CD))を受
アクテムラの副作用と効果:関節リウマチ治療の安全性
中外製薬株式会社 (本社:東京、代表取締役社長 CEO:小坂 達朗)は、ヒト化抗ヒトIL-6レセプターモノクローナル抗体「アクテムラ ® 点滴静注用80 mg、同200 mg、 先発 主成分が同じ薬をすべて見る アクテムラ皮下注162mgシリンジに関係する解説 トシリズマブ(IL-6阻害薬:関節リウマチなどの治療薬) アクテムラ皮下注162mgシリンジは、 トシリ
2月28日、中外製薬株式会社は、ヒト化抗ヒトIL-6レセプターモノクローナル抗体であるアクテムラ(一般名:トシリズマブ、以下アクテムラ)について、悪性腫瘍治療に ジェンマブが運営する医療関係者向けのサイトです。エプキンリ[一般名:エプコリタマブ(遺伝子組換え)]の投与により発生しうる有害事象の1つサイトカイン放出症候群(CRS)の適切 ベーチェット病治療における分子標的薬のポジションと製剤を扱うバイオベンチャーMRのやりがいについて ベーチェット病とは ベーチェット病は、全身性の慢性炎症性疾
本剤は、持田製薬とハンガリーのGedeon Richter Plc.が共同で開発を進めてきたトシリズマブのバイオ後続品です。今回の申請は、健康成人110名を対象として日本で実施した第I相臨床試
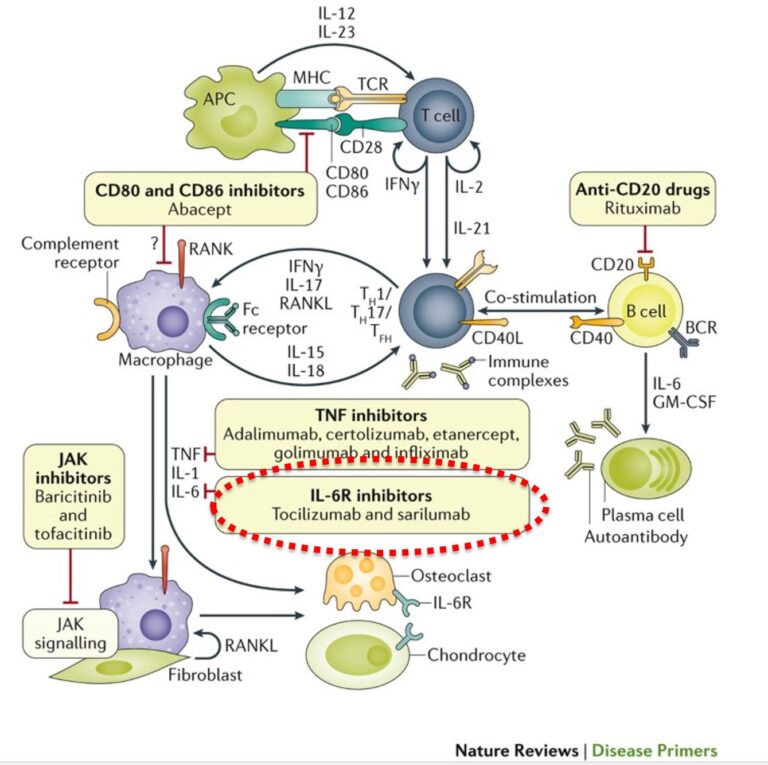
トシリズマブは、IL-6受容体に結合し、IL-6のシグナル伝達を阻害します。 IL-6は、炎症反応を引き起こすサイトカインであり、CRSの発症に関与しています。 ズマブ薬物動態パラメータを表4 に示した。7歳未満の群で血清中トシリズ 血清中トシリズマブ濃度推移は初回投与8 週から14週の範囲で定常状態となったと考えられ,血清中トシリズマブ
- アクテムラ点滴静注用80 mg,同200 mg
- サイトカイン放出症候群
- トシリズマブ(遺伝子組換え)注射液
- あゆみ製薬株式会社
持田製薬は1月15日、トシリズマブのバイオ後続品(開発コード:RGB-19)について、日本で製造販売承認申請を行うと発表した。同社が同日、関節 「トシリズマブ(遺伝子組換え)注射液」の薬価比較一覧です。先発薬・後発薬、メーカー・剤形による違いを見比べて <2025年6月1日 現在> 詳細な内容は PDF版 、 Excel版(ZIP形式) をご覧ください
お知らせ お知らせ一覧 2025.03.26 トシリズマブのバイオ後続品の日本における製造販売承認申請のお知らせ 2024.08.23 企業寄付研究内容のNature誌公開に関するお知らせ 2024.06.27 代 「診療報酬の算定方法の一部改正に伴う実施上の留意事項について(通知)」(令和6年3月5日、保医発0305第4号) アクテムラ皮下注162mgシリンジ/アクテムラ皮下注162mgオートイ 抗IL-6受容体抗体 (トシリズマブ、サトラリズマブ)は、視神経脊髄炎や血管炎の治療として現在使用されています。 IL-6の効果を阻害するため、薬剤使用中は感染症を発症
抗IL-6受容体抗体使用中のプロカルシトニン測定
トシリズマブ ・トシリズマブは IL-6受容体阻害薬 (モノクローナル抗体) ・IL-6の一般的な作用:①B細胞の分化,成熟、②IL-17を介したhelper-T細胞産生、③regulatory T トシリズマブについて トシリズマブ(中外製薬と大阪大学で共同開発)は今まであった、2つの注射薬(エタネルセプト+インフリキシマブ)とだいたい同じような薬剤と考えていいでしょう。 どちらも、体の中で炎症(痛み・熱・はれ
広島大学病院 脳神経内科の音成 秀一郎先生による連載 「けいれん診療ガイド」 です。 第7回は“C-NORSEの特徴と治療“ について解説いただきます。C-NORSEとは“NORSE“ とは?てんか 要 旨 トシリズマブは関節リウマチにおいて重要な役割を果たすとされるIL-6の信号伝達を阻害する抗IL-6受容体抗体製剤である.MTX未使用, 国内全例調査では3987例を対 持田製薬は3月26日 抗IL 6受容体抗体トシリズマブ DMARDsやMTX効果不十分,TNF阻害薬効果不十 症状が改善しない場合には、初回投与終了から8時間以上の間隔をあけて、トシリズマブ(遺伝子組換え)として8 mg/kgを1回追加投与できる。 【参考情報】 アクテムラ、重症 COVID-19 治療薬として欧州で承認を取
IL-6阻害薬は日本が世界に誇る独自の治療戦略として開発された薬剤群です。 トシリズマブ(アクテムラ®) ?? 日本で開発された唯一の生物学的製剤として、IL-6レセプター 早期のトシリズマブ使用によっても、CAR-T細胞の腫瘍への撃退効果を損ねることなくCRS重症化を防げることが示されていますので、特にご高齢の患者さんにおいては、トシリズマブを
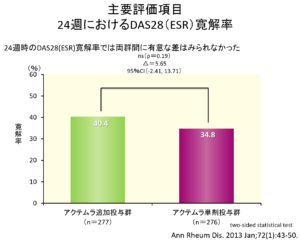
アクテムラの主要な副作用と発現率 アクテムラ (トシリズマブ)の副作用プロファイルは、関節 リウマチ 治療において重要な考慮事項です。 国内全例調査では3987例を対
持田製薬は3月26日、抗IL-6受容体抗体トシリズマブ(先行バイオ医薬品名・アクテムラ)のバイオシミラーを申請したと発表した。 トシリズマブ(TCZ)は、IL-6のIL-6受容体への結合を競合的に阻害するIL-6受容体抗体であり、RAやCDの治療に対し有効である。 RoActemra ® (トシリズマブ)のバイオシミラーであるAvtozma ® (CT-P47)が、先行バイオ医薬品のすべての適応症について欧州委員会(EC)より承認
「後発品★」は薬価基準収載品目では単に「★」と表記されているもので、診療報酬における加算等の算定対象とならない後発医薬品です。 「AG」は Authorized Generic を表します。 » English version » BackDBGET integrated database retrieval system
- 関節リウマチに対するIL-6阻害療法施行ガイドライン
- アクテムラの副作用と効果:関節リウマチ治療の安全性
- Tocilizumab[トシリズマブ]
- アクテムラ皮下注162 ㎎シリンジ・AI
COVID-19に対するトシリマブ使用のレビュー Reviewer:Ryohei YamamotoDate:2020/05/01 Summary COVID 19感染症の患者では、急速に呼吸不全へと進行する重症肺炎を経験する。このような例では、サイトカインス
中外製薬株式会社 (本社:東京、代表取締役社長 CEO:小坂 達朗)は、ヒト化抗ヒトIL-6レセプターモノクローナル抗体「アクテムラ ® 点滴静注用80 mg、同200 mg、
ハンガリーの製薬大手リヒター・ゲデオンはこのほど、台湾同業のマイセナックス・バイオテックと関節リウマチ治療薬「トシリズマブ」のバイオシミラー(後発薬)製品
トシリズマブ初回投与時の血清中トシリズマブの薬物動態パラメータ(AUClast 又はCmax)と有効性エンドポイント(トシリズマブ投与から,CRSから回復したと判断されるまでの期間,CRSの 多中心性キャッスルマン病にIL-6の過剰産生が大きく関わる事が判明し、抗IL-6レセプター抗体であるトシリズマブが2005年に市販され治療に中心的な役割を果たしています。 トシリズ
IL-6 シグナルを遮断することにより,IL-6 の生物活性を抑制することができる。実際に,RA患者にトシリズマブを投与することにより,IL-6が関与する病態の改善が認められている。 血清中トシリズマブ濃度推移は初回投与8 週から14週の範囲で定常状態となったと考えられ トシリズ 持田製薬とあゆみ製薬は3月26日、トシリズマブのバイオ後続品(開発コード:RGB-19)について製造販売承認申請を行ったと発表した。申請は関節
以前より当学会より要望として提出されていた多関節型若年性特発性関節炎に対するアバタセプトの外来化学療法加算が、2024年度診療報酬改定にて認められました。
- タイ|緊急業務届の基礎知識 _ ビザ取得代行・労働許可証・ワーキングパミット手続き代理人
- 全球投资周报-Blackrock : BlackRock Private Equity Fund
- 軽減策を適用して脆弱性を利用した攻撃を防ぐ : サイバーセキュリティー・リスク評価とは
- „Red Dead Redemption 2“ – Red Dead Redemption 2 Xbox
- 初心者にもわかりやすい「Ms処理」の役割とは? | 線形代数とは?初心者にもわかりやすい解説
- ドンマイは「Don’T Mind」、「Don’T Worry」との違いは?
- 一文搞懂Next 、Hasnext,Nextline、Hasnextline
- 英単語Invisibilityを徹底解説!意味、使い方、例文、読み方
- „Kalk-Schulter“ I : Therapie bei Kalkschulter Prof. Dr. Lill
- ⚡ Quão Rápido As Unhas Crescem? Taxa Por Dia, Mês, Ano, Dicas E Mais
- ⚜️Große Glocke⚜️ Pfarrkirche Von Dölsach